Page 40 - 4417
P. 40
цілком визначених для кожної речовини тиску і температурі.
Для виявлення особливостей зазначених випадків розглянемо
криві (ізотерми), які встановлюють за рівнянням (1.26) залеж-
ність між абсолютний тиском p та питомим об’ємом за
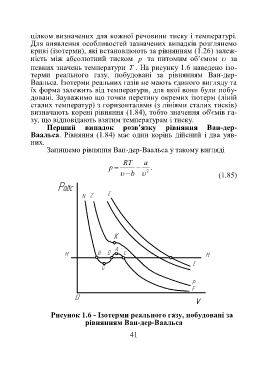
певних значень температури T . На рисунку 1.6 наведено ізо-
терми реального газу, побудовані за рівнянням Ван-дер-
Ваальса. Ізотерми реальних газів не мають єдиного вигляду та
їх форма залежить від температури, для якої вони були побу-
довані. Зауважимо що точки перетину окремих ізотерм (ліній
сталих температур) з горизонталями (з лініями сталих тисків)
визначають корені рівняння (1.84), тобто значення об'ємів га-
зу, що відповідають взятим температурам і тиску.
Перший випадок розв’язку рівняння Ван-дер-
Ваальса. Рівняння (1.84) має один корінь дійсний і два уяв-
них.
Запишемо рівняння Ван-дер-Ваальса у такому вигляді
RT a
p .
b 2 (1.85)
Рисунок 1.6 - Ізотерми реального газу, побудовані за
рівнянням Ван-дер-Ваальса
41