Page 92 - 6375
P. 92
для дослідження найбільш характерних особливих станів речовини. Одним з них є так
званий критичний стан. На рис. 6 зображено експериментальну ізотерму і ізотерму
Ван-дер-Ваальса для докритичного стану реального газу.
Докритичні ізотерми Ван-дер-Ваальса замість горизонтальної ділянки, яка відповідає
фазовому переходу «газ – рідина», мають хвилеподібну ділянку . Вона зумовлена так
званими метастабільними станами – станами системи, коли певні нескінченно малі дії
спричиняють нескінченно малі зміни стану, а інші нескінченно малі дії – скінченні зміни
стану системи.
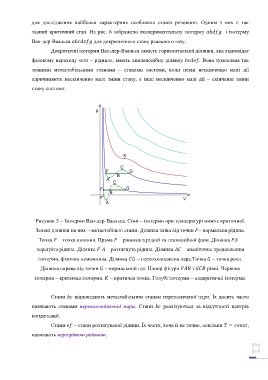
Рисунок 5 – Ізотерми Ван-дер-Ваальса. Сині – ізотерми при температурі нижче критичної.
Зелені ділянки на них – метастабільні стани. Ділянка зліва від точки – нормальна рідина.
Точка – точка кипіння. Пряма – рівновага рідкої та газоподібної фази. Ділянка –
′
перегріта рідина. Ділянка – розтягнута рідина. Ділянка – аналітичне продовження
ізотерми, фізично неможлива. Ділянка – переохолоджена пара.Точка – точка роси.
Ділянка справа від точки – нормальний газ. Площі фігури і рівні. Червона
ізотерма – критична ізотерма. – критична точка. Голубі ізотерми – надкритичні ізотерми.
Стани відповідають метастабільним станам перенасиченої пари. Їх досить часто
називають станами переохолодженої пари. Стани реалізуються за відсутності центрів
конденсації.
Стани – стани розтягуваної рідини. Їх часто, хоча й не точно, оскільки = ,
називають перегрітою рідиною.