Page 112 - 6140
P. 112
Натрій гідрофосфат Na2HPO4 утворює зелений осад
Ni3(PO4)2, розчинний в кислотах, у тому числі і в ацетатній
кислоті. Осад розчинний також в аміаку, але не розчиняється в
лугах.
Аналіз суміші катіонів I-VI аналітичних груп,
заснований на кислотно-основній класифікації, починають
звичайно з виявлення іона амонію дробним методом.
Систематичний аналіз починають із осадження й
відділення хлоридів катіонів II аналітичної групи. Потім
переводять в осад і відокремлюють сульфати катіонів III
аналітичної групи. При обробці розчину, отриманого після
осадження катіонів II і III аналітичних груп, надлишком
розчину натрій гідроксиду в осад переводять основні по своїй
природі гідроксиди катіонів V і VI груп, а в розчині
залишаються катіони IV аналітичної групи у вигляді
відповідних гідроксокомплексів.
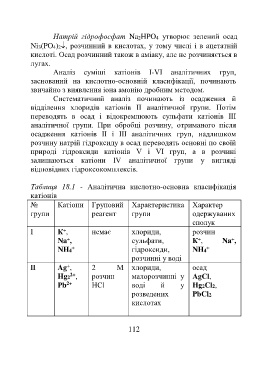
Таблиця 18.1 - Аналітична кислотно-основна класифікація
катіонів
№ Катіони Груповий Характеристика Характер
групи реагент групи одержуваних
сполук
+
I К , немає хлориди, розчин
+
+
Na , сульфати, К , Na ,
+
+ +
NH4 гідроксиди, NH4
розчинні у воді
+
II Ag , 2 М хлориди, осад
2+
Hg2 , розчин малорозчинні у AgСl,
Pb 2+ НСl воді й у Hg2Cl2,
розведених PbCl2
кислотах
112