Page 125 - 6141
P. 125
- 3
pOH= -lg[OH ] = -lg4,8 10 3 lg 8 , 4 3 , 2
pH = 14 – pOH = 14 – 2,3 = 11,7
Одержані дані заносять в таблицю 6.1.
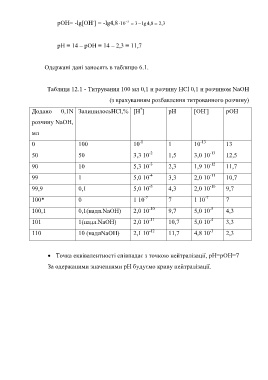
Таблиця 12.1 - Титрування 100 мл 0,1 н розчину HCl 0,1 н розчином NaOH
(з врахуванням розбавлення титрованного розчину)
-
+
Додано 0,1N ЗалишилосьHCl,% [H ] pH [OH ] pOH
розчину NaOH,
мл
-13
-1
0 100 10 1 10 13
-13
-2
50 50 3,3 10 1,5 3,0 10 12,5
-12
-3
90 10 5,3 10 2,3 1,9 10 11,7
-11
-4
99 1 5,0 10 3,3 2,0 10 10,7
-5 -10
99,9 0,1 5,0 10 4,3 2,0 10 9,7
-7
-7
100* 0 1 10 7 1 10 7
-10
-5
100,1 0,1(надл.NaOH) 2,0 10 9,7 5,0 10 4,3
-11 -4
101 1(надл.NaOH) 2,0 10 10,7 5,0 10 3,3
-3
-12
110 10 (надлNaOH) 2,1 10 11,7 4,8 10 2,3
Точка еквівалентності співпадає з точкою нейтралізації, рН=рОН=7
За одержаними значеннями рН будуємо криву нейтралізації.